Trong hệ thống canh tác hiện đại, đặc biệt là mô hình nhà màng sử dụng tưới nhỏ giọt, nông dân thường ưu tiên sử dụng các loại phân đơn tinh khiết như Canxi nitrat, Magie sulfat và các vi lượng chelate để phối trộn thành dung dịch dinh dưỡng. Các nguyên tố này đại diện cho ba nhóm chính: Nitrate (NO₃⁻), Sulphate (SO₄²⁻) và Chelate (Fe-EDTA, Zn-DTPA…) – mỗi nhóm mang vai trò thiết yếu trong sự phát triển và trao đổi chất của cây trồng.
Tuy nhiên, điều mà nhiều người trồng chưa nhận ra là sự tương tác hóa học giữa các nhóm ion này có thể ảnh hưởng mạnh mẽ tới khả năng hấp thu dinh dưỡng, thậm chí làm giảm hiệu quả phân bón dù công thức pha vẫn “đủ liều”.
Một ví dụ điển hình là khi Bo hoặc Chelate vi lượng bị “giữ lại” do kết tủa với ion Ca²⁺ hoặc bị phá vỡ bởi môi trường chứa quá nhiều sulphate. Tương tự, đạm dạng nitrate nếu dùng quá mức cũng có thể gây xung đột trong quá trình vận chuyển vi lượng như Fe, Zn…
Bài viết này sẽ giúp bạn hiểu rõ cơ chế tương tác giữa Nitrate – Sulphate – Chelate, từ đó tối ưu cách phối trộn, điều chỉnh thời điểm tưới, và tăng hiệu suất hấp thu dinh dưỡng mà không làm hại hệ thống.
1️⃣ Nitrate (NO₃⁻) – đạm nhanh và vai trò làm “chất dẫn”
Trong số các dạng đạm thường dùng, Nitrate (NO₃⁻) là hình thức được cây hấp thu nhanh nhất, ít gây độc và ít ảnh hưởng đến pH môi trường rễ so với ammonium (NH₄⁺). Chính vì vậy, các loại phân như Canxi nitrat (Ca(NO₃)₂) và Kali nitrat (KNO₃) luôn được ưu tiên trong các công thức dinh dưỡng cho dưa lưới, đặc biệt ở giai đoạn sinh trưởng mạnh.
Tuy nhiên, ngoài vai trò cung cấp đạm, Nitrate còn mang đặc tính đặc biệt: nó là một anion mạnh, có thể kéo theo các cation đi cùng trong quá trình vận chuyển qua màng rễ. Điều này có nghĩa là, khi cây hấp thu NO₃⁻, nó đồng thời kéo theo Ca²⁺, Mg²⁺, K⁺ để cân bằng điện tích. Đây là hiện tượng mang lại lợi ích rõ ràng khi sử dụng Canxi nitrat – cây vừa nhận được đạm, vừa hấp thu được Canxi dễ dàng hơn.
Tuy nhiên, nồng độ NO₃⁻ quá cao cũng có thể trở thành vấn đề. Trong môi trường dung dịch có nhiều Nitrate, cây ưu tiên hút anion NO₃⁻ và các cation đi kèm, đồng thời ức chế hấp thu các nguyên tố vi lượng dạng ion hóa như Fe²⁺, Zn²⁺, Mn²⁺ – vốn không tham gia vào cặp vận chuyển đồng thời với NO₃⁻. Hiện tượng này được gọi là cạnh tranh hấp thu theo cơ chế điện hóa.
Điều này lý giải vì sao trong nhiều trường hợp, dù công thức đã bổ sung đầy đủ vi lượng, nhưng cây vẫn có dấu hiệu thiếu sắt (lá non vàng giữa gân), thiếu kẽm (lá nhỏ, chồi yếu) – mà nguyên nhân nằm ở việc đạm nitrate quá dư, gây cản trở hấp thu chéo.
Do đó, khi sử dụng các loại phân chứa NO₃⁻, người trồng cần lưu ý đến:
- Liều lượng hợp lý, tránh dùng nitrate quá dày trong suốt chu kỳ cây
- Phối hợp xen kẽ với các nhóm dinh dưỡng khác, đặc biệt là vi lượng chelate hoặc Bo – nên tưới cách thời điểm để tránh xung đột
Việc hiểu rõ vai trò “kép” của NO₃⁻ – vừa là nguồn đạm, vừa là “chất dẫn” – sẽ giúp người trồng chủ động hơn trong điều chỉnh công thức, không chỉ theo biểu hiện cây mà còn theo nguyên tắc sinh lý dinh dưỡng.
2️⃣ Sulphate (SO₄²⁻) – trung lượng thiết yếu, nhưng dễ gây kết tủa
Sulphate (SO₄²⁻) là dạng anion mang lưu huỳnh phổ biến trong nông nghiệp, thường gặp trong các loại phân như Magie sulfat (MgSO₄.7H₂O), Kali sulfat (K₂SO₄) hoặc vi lượng dạng sulfat (ZnSO₄, FeSO₄…). Dù chỉ chiếm một phần nhỏ trong tổng công thức, nhưng Sulphate đóng vai trò cực kỳ quan trọng trong chu trình tổng hợp amino acid chứa lưu huỳnh, giúp cây tăng cường sức đề kháng, hương vị trái và khả năng chuyển hóa đạm.
Tuy nhiên, điều khiến SO₄²⁻ trở thành “con dao hai lưỡi” là do khả năng phản ứng với các cation hóa trị cao như Ca²⁺, Fe²⁺, Mn²⁺, tạo thành các muối ít tan hoặc không tan trong dung dịch. Trong điều kiện pH > 6.5 hoặc nước có độ cứng cao, các phản ứng kết tủa như:
- Ca²⁺ + SO₄²⁻ → CaSO₄↓ (thạch cao)
- Fe²⁺ + SO₄²⁻ → FeSO₄↓ (sắt(II) sulfat, dễ kết tinh khi để lắng)
…sẽ xảy ra nhanh chóng và gây nghẹt đường ống nhỏ giọt hoặc làm mất hoạt tính phân bón.
Ngoài ra, SO₄²⁻ còn có tính axit nhẹ, nên khi dùng với nồng độ cao sẽ hạ pH của dung dịch tưới, làm ảnh hưởng đến độ bền của vi lượng chelate – đặc biệt là nhóm chelate dễ mất ổn định như Fe-EDTA. Trong môi trường pH < 5.5, một phần chelate có thể bị phá vỡ, khiến ion Fe²⁺ tự do dễ bị oxy hóa thành Fe³⁺ và kết tủa.
Tóm lại, Sulphate là trung lượng cần thiết nhưng nhạy cảm:
- Dùng đúng: giúp cây xanh lá, tích đạm, tạo mùi thơm
- Dùng sai: gây kết tủa, cạnh tranh vi lượng, rối loạn pH
Người trồng cần lưu ý:
- Không pha Sulphate cùng lúc với Canxi hoặc vi lượng chelate
- Luôn đưa Sulphate vào bồn B, cách xa các phân chứa Ca²⁺
- Không lạm dụng các loại phân vi lượng dạng sulfat thô – dễ lắng và khó kiểm soát
Việc điều chỉnh thời điểm tưới và cách tách bồn hợp lý sẽ giúp phát huy hiệu quả của SO₄²⁻ mà không đánh đổi bằng rủi ro kỹ thuật hay giảm hấp thu vi lượng.
3️⃣ Vi lượng chelate – dễ bị “phá vỡ” nếu môi trường bất lợi
Trong môi trường canh tác chính xác như nhà màng hoặc hệ thống tưới nhỏ giọt, vi lượng chelate (Fe, Zn, Mn, Cu…) là lựa chọn gần như bắt buộc nếu muốn duy trì nồng độ ổn định, tránh mất hiệu lực do kết tủa hoặc bị cố định trong giá thể. Dạng chelate giúp bao bọc ion kim loại, ngăn không cho chúng phản ứng với các gốc anion khác trong dung dịch như OH⁻, SO₄²⁻, HPO₄²⁻…
Tuy nhiên, không phải mọi chelate đều ổn định như nhau. Fe-EDTA, chẳng hạn, chỉ giữ được độ bền trong môi trường pH dưới 6.5. Khi pH vượt ngưỡng, hoặc trong điều kiện có nhiều ion phản ứng mạnh như Ca²⁺, SO₄²⁻, liên kết chelate dễ bị thay thế, khiến ion Fe²⁺ trở nên tự do. Trong môi trường giàu oxy như dung dịch tưới, Fe²⁺ bị oxy hóa thành Fe³⁺ – dạng này không tan, tạo ra cặn nâu kết tủa và gây tắc béc tưới nhỏ giọt.
Tương tự, Zn-EDTA hay Mn-EDTA cũng có thể bị cạnh tranh bởi các anion mạnh như NO₃⁻ hoặc SO₄²⁻, nhất là khi liều lượng các anion này vượt mức cần thiết. Khi bị cạnh tranh, các vi lượng không còn bám vào chelate mà bị thất thoát, dẫn đến hiện tượng cây thiếu vi lượng dù công thức vẫn đủ trên lý thuyết.
Một điểm đáng lưu ý nữa là: Chelate không phải là “chống kết tủa vĩnh viễn”. Nếu điều kiện dung dịch không phù hợp (pH, nhiệt độ, ion đối kháng cao), liên kết chelate vẫn bị phá vỡ, khiến vi lượng trở nên khó hấp thu, dễ bị lắng hoặc mất hoạt tính sinh học.
Vì vậy, để sử dụng hiệu quả vi lượng chelate, cần:
- Pha vào bồn riêng (thường là bồn B), không chung với Canxi hoặc Sulphate
- Chọn loại chelate phù hợp với pH môi trường:
- Fe-EDTA: dùng khi pH < 6.5
- Fe-DTPA: ổn định hơn, dùng cho pH < 7.5
- Fe-EDDHA: bền nhất, dùng được tới pH 8.0
- Không pha cùng lúc với phân có khả năng làm hạ pH quá mạnh (như MAP, axit humic…)
Tóm lại, chelate chỉ phát huy tối đa hiệu quả khi được đặt đúng vị trí, đúng điều kiện. Nếu không, người trồng dễ rơi vào “bẫy tâm lý”: nghĩ rằng đã cung cấp đủ vi lượng, nhưng thực tế cây vẫn thiếu – một cách âm thầm và khó phát hiện sớm.
4️⃣ Tương tác chéo – cạnh tranh hoặc hỗ trợ giữa các ion
Sau khi đã phân tích từng nhóm riêng lẻ, chúng ta cần nhìn vào bức tranh tổng thể: khi Nitrate, Sulphate và Chelate cùng tồn tại trong dung dịch, chúng không hoạt động độc lập, mà thường tạo ra hiệu ứng tương tác chéo, có thể là hỗ trợ hoặc ức chế lẫn nhau. Hiểu rõ những tương tác này sẽ giúp người trồng chủ động điều chỉnh công thức và lịch tưới phù hợp hơn. ✅ Tương tác hỗ trợ: khi ion này giúp tăng hấp thu của ion khác Nitrate (NO₃⁻) giúp kéo theo Ca²⁺ và Mg²⁺ nhờ hiệu ứng cân bằng điện tích khi cây hút ion âm → đây là lý do tại sao Canxi nitrat thường được pha chung với Magie sulfat, đặc biệt ở giai đoạn nuôi thân, nuôi lá. Khi phối hợp ở nồng độ hợp lý, Chelate Zn-EDTA hoặc Mn-EDTA có thể hoạt động tốt trong môi trường chứa NO₃⁻, vì nitrate không phản ứng trực tiếp với vi lượng và giúp duy trì dòng hút ion ổn định. ❌ Tương tác đối kháng: khi ion này gây cản trở hoặc kết tủa với ion khác SO₄²⁻ + Ca²⁺ → CaSO₄↓ (thạch cao): kết tủa gây nghẹt béc SO₄²⁻ + Fe²⁺/Zn²⁺ → tạo muối khó tan hoặc kết tinh khi pH cao Ca²⁺ + Bo (solubor) → tạo borat canxi, kết tinh mạnh khi pH > 6.5
Chelate + SO₄²⁻: có thể bị phá vỡ chelate, làm giảm hiệu lực vi lượng
Khi NO₃⁻ dư quá mức, sẽ gây cạnh tranh hấp thu với Zn²⁺, Fe²⁺, do ưu tiên vận chuyển các cation đi kèm với nitrate → làm vi lượng bị “ra rìa”, hấp thu chậm hoặc không hấp thu.
⚖️ Tóm tắt nguyên tắc “đi chung – tách riêng”:
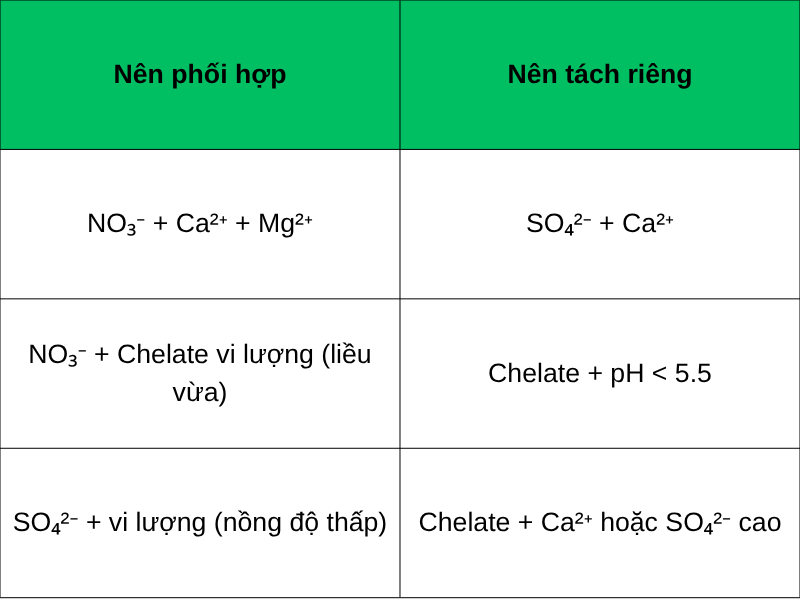
Thay vì loại bỏ hoàn toàn nhóm này hay nhóm kia, cách tiếp cận đúng là điều tiết liều lượng và thời điểm tưới, để cây hấp thu tối đa từng thành phần mà không tạo phản ứng hóa học bất lợi.
5️⃣ Gợi ý cách phối trộn và tưới theo thời điểm để giảm xung đột
Sau khi đã hiểu rõ cơ chế tương tác và cạnh tranh giữa Nitrate – Sulphate – Chelate, bước quan trọng tiếp theo là chuyển hóa kiến thức đó thành lịch tưới – lịch phối trộn cụ thể, phù hợp với điều kiện canh tác thực tế và cấu hình hệ thống của từng vườn.
🕘 Chia thời điểm tưới theo nhóm ion
Một trong những cách hiệu quả nhất để hạn chế phản ứng bất lợi là tưới luân phiên theo nhóm phân – đặc biệt khi hệ thống không có bồn A – B riêng biệt. Cụ thể:
- Buổi sáng (hoặc cách ngày 1–3 lần/tuần)
→ Ưu tiên nhóm Nitrate + Canxi + Magie
→ Ví dụ: Canxi nitrat + MgSO₄.7H₂O (liều phù hợp giai đoạn sinh trưởng) - Buổi chiều (hoặc luân phiên với sáng)
→ Dùng nhóm Sulphate + Chelate vi lượng + Bo
→ Ví dụ: MgSO₄ + Solubor + Zn-EDTA + Fe-DTPA
Việc tách thời điểm tưới không chỉ giúp hạn chế kết tủa, mà còn tạo khoảng “giải lập ion” trong vùng rễ – giúp cây hấp thu mượt mà từng nhóm dinh dưỡng mà không bị cạnh tranh khốc liệt.
💡 Nếu hệ thống có bồn A – B, ưu tiên tách như sau:
- Bồn A: Chứa Nitrate (NO₃⁻) và các cation ổn định:
→ Canxi nitrat, Kali nitrat, Magie sulfat (liều thấp) - Bồn B: Chứa các ion dễ phản ứng hoặc kém bền:
→ Bo (Solubor), Chelate vi lượng (Fe, Zn, Mn…), K₂SO₄, MKP, MAP
Tuyệt đối không trộn chung Ca²⁺ với SO₄²⁻ hoặc Bo
Kiểm tra EC – pH thường xuyên, điều chỉnh pH dung dịch ở ngưỡng 5.8 – 6.2 để đảm bảo chelate hoạt động ổn định
📌 Gợi ý lịch phối hợp theo giai đoạn sinh trưởng của cây:
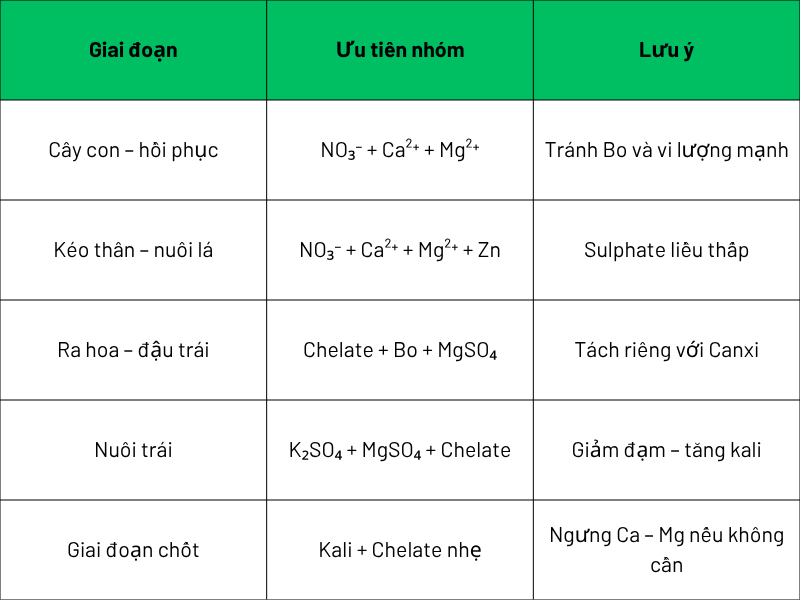
Tổng kết
Sự tương tác giữa Nitrate – Sulphate – Chelate là một phần nhỏ trong hóa học dinh dưỡng, nhưng lại có ảnh hưởng rất lớn đến hiệu suất sử dụng phân bón, khả năng hấp thu vi lượng và tuổi thọ của hệ thống tưới. Canh tác hiện đại không dừng ở việc “bón đúng loại”, mà còn cần hiểu đúng “tính cách” của từng nhóm ion để phối hợp nhịp nhàng.
Với những gợi ý trên, người trồng có thể từng bước kiểm soát tốt hệ dinh dưỡng, tránh sai lầm thường gặp, và từ đó tối ưu sản lượng – chất lượng – độ bền của cả hệ thống.
⏩⏩ Mời quý vị và các bạn quan tâm theo dõi các nền tảng truyền thông để tìm hiểu, trao đổi và chia sẻ thêm về các kinh nghiệm trong đầu tư và sản xuất nông nghiệp cùng cộng đồng và chuyên gia tại:
- Youtube: Youtube.com/@Kythuattrongcayvn
- Facebook Page: Facebook.com/kythuattrongcay.vn/
- Facebook Group: Facebook.com/6441565519262518
- Tiktok: Tiktok.com/@kythuattrongcay.vn


